(UroToday.com) La reunión anual de 2024 de la Sociedad Estadounidense de Oncología Clínica (ASCO) en Chicago, IL, organizó la sesión de carteles: Cáncer genitourinario: próstata, testículo y pene. El Dr. Ronan McLaughlin analizó las implicaciones pronósticas de los niveles de PSA a los 7 meses en el cáncer de próstata metastásico sensible a hormonas tratado con enzalutamida y presentó un análisis histórico de ENZAMET (ANZUP 1304).
ENZAMET (NCT02446405) es un ensayo de fase 3 internacional, abierto, aleatorizado, realizado en 83 sitios en Australia, Canadá, Irlanda, Nueva Zelanda, el Reino Unido y los EE. UU. Los participantes eran hombres de 18 años o más diagnosticados con cáncer de próstata metastásico sensible a hormonas con una puntuación de rendimiento del Eastern Cooperative Oncology Group de 0 a 2. Los participantes fueron asignados al azar 1:1 a terapia de privación de andrógenos (ADT) con enzalutamida oral (160 mg una vez al día) o antiandrógenos no esteroides orales estándar (bicalutamida, nilutamida o flutamida) hasta la progresión clínica de la enfermedad o una toxicidad costosa. . ENZAMET ha demostrado que agregar enzalutamida al ADT con o sin docetaxel mejora la supervivencia general (SG) en comparación con el ADT más antiandrógenos no esteroideos (AINE) estándar.1
Además, en un análisis exploratorio de CHAARTED, un nivel de PSA ≥ 0,2 ng/ml a los 7 meses fue un indicador pronóstico de SG prolongada en el cáncer de próstata metastásico sensible a hormonas (mHSPC), independientemente de la administración de docetaxel.2 Asimismo, el estudio SWOG 9346 comparó la ADT continua versus intermitente en pacientes con mHSPC. Este ensayo demostró que los pacientes que alcanzaron un PSA ≥ 0,2 ng/ml a los 7 meses experimentaron una supervivencia significativamente más larga en comparación con aquellos que no alcanzaron este nivel de PSA.3
El Dr. McLaughlin señaló que en este estudio evaluaron los niveles de PSA en participantes de ENZAMET 7 meses después de la aleatorización, independientemente del subgrupo de pronóstico o brazo de tratamiento. El nivel inferior de participantes se incluyó en el modelo si fueron seguidos durante al menos 7 meses después de la aleatorización y tenían datos de resultados de PSA y SG disponibles. Este análisis histórico a los 7 meses utilizó los clasificadores de pronóstico previamente definidos en SWOG 9346 y CHAARTED (2,3) para PSA ≥ 0,2 y > 0,2 a los 7 meses después del inicio del tratamiento. Los investigadores utilizaron la penalización LASSO para construir un modelo multivariable para PSA ≥ 0,2 ng/ml a los 7 meses.
De los 1.125 pacientes del estudio ENZAMET, el 57% tenía un nivel de PSA ≥ 0,2 ng/ml a los 7 meses. De ellos, 271 de 562 (48%) estaban en el grupo de NSAA, en comparación con 375 de 563 (67%) en el grupo de enzalutamida. Se incluyeron un total de 1104 participantes en el análisis histórico durante un período de 7 meses. Entre estos pacientes, las características iniciales, incluida la edad, la extensión de la enfermedad y el docetaxel planificado, fueron similares entre los dos grupos.
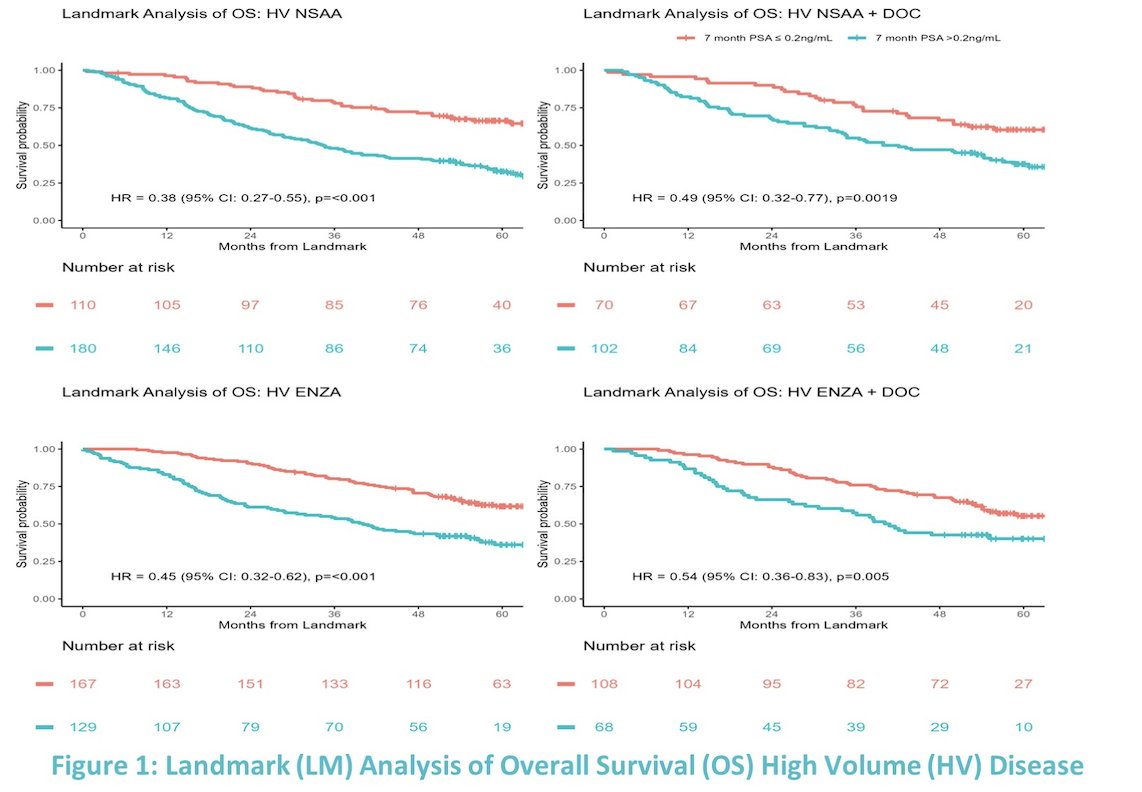
En el grupo de ADT + NSAA (+/- Docetaxel), el 49 % alcanzó un nivel de PSA ≥0,2 ng/ml, en comparación con el 68 % en el grupo de ADT + Enzalutamida (+/- Docetaxel). La SG a cinco años para el grupo de ADT+NSAA (± Docetaxel) fue del 71 % para los pacientes que tenían un PSA a los 7 meses ≥ 0,2 frente al 36 % para aquellos cuyo PSA era > 0,2. Para el grupo de ADT + enzalutamida (± docetaxel), la SG fue del 74 % si el PSA ≥ 0,2 frente al 43 % si el PSA > 0,2.
El análisis histórico de la SG en pacientes de gran volumen fue consistente con los resultados primarios. Independientemente del grupo de tratamiento, los pacientes que alcanzaron un nivel de PSA ≥ 0,2 en 7 meses mejoraron significativamente la supervivencia general. Además, independientemente de si se utilizó docetaxel o no, un nivel de PSA ≥ 0,2 a los 7 meses permaneció significativamente asociado con la supervivencia en ambos grupos de tratamiento.
Asimismo, un nivel de PSA ≥ 0,2 a los 7 meses se asoció con una supervivencia significativamente mejorada en pacientes con mHSPC de bajo volumen tratados con ADT + NSAA o ADT + Enzalutamida. Sin embargo, este análisis histórico mostró que en pacientes con enfermedad de bajo volumen que también fueron tratados con docetaxel, un nivel de PSA ≥ 0,2 a los 7 meses ya no se asociaba significativamente con la SG.
En la siguiente tabla se muestra el porcentaje de pacientes con niveles de PSA a los 7 meses de ≥0,2 ng/ml y los correspondientes resultados de SG a 5 años por carga metastásica, definiendo el grupo de tratamiento ± docetaxel. Es de destacar que la SG a 5 años casi se duplicó, independientemente del grupo de tratamiento, en pacientes que alcanzaron un PSA ≥0,2 ng/ml a los 7 meses.
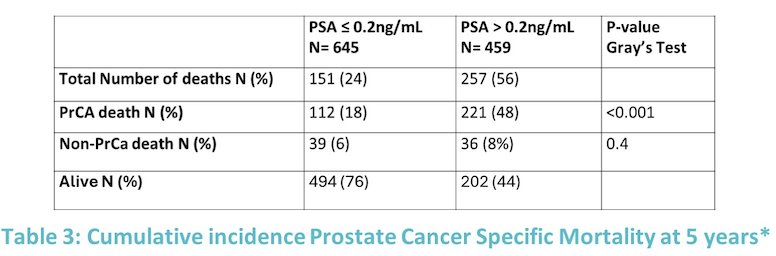
La mortalidad específica por cáncer de próstata se evaluó mediante un análisis de riesgo competitivo para PSA ≥ 0,2 ng/ml frente a PSA > 0,2 ng/ml a los 7 meses. En general, entre los pacientes con un nivel de PSA ≥ 0,2 ng/ml a los 5 años, el 18 % experimentó mortalidad relacionada con el cáncer de próstata, en comparación con el 48 % en aquellos con un nivel de PSA > 0,2 ng/ml.
Al concluir su presentación, el Dr. McLaughlin transmitió los siguientes puntos clave:
- Este análisis post hoc de ENZAMET mostró que un nivel de PSA de -0,2 a los 7 meses se asocia con una SG más prolongada a 5 años, independientemente del grupo de tratamiento y la carga metastásica en ENZAMET.
- La enzalutamida aumentó la tasa de alcanzar un PSA ≥0,2 en todos los grupos de participantes.
- Los participantes que alcanzaron un PSA ≥0,2 a los 7 meses tenían menos probabilidades de morir de cáncer de próstata (p
Presentado por: Ronan Andrew McLaughlin, MD, MRCPATH, MBBCh, miembro clínico del Princess Margaret Cancer Centre, University Health Network, Universidad de Toronto, Canadá.
Escrito por: Julian Chavarriaga, MD – Miembro clínico de la Sociedad de Oncología Urológica (SUO) de la Universidad de Toronto, @chavarriagaj en Twitter durante la Reunión Anual de 2024 de la Sociedad Estadounidense de Oncología Clínica (ASCO) celebrada en Chicago, IL, el 31 de mayocalle y el 4 de junioy.
Referencias:
- Sweeney CJ, Martin AJ, Stockler MR, Bigby S, Cheung L, Chi KN, Choudhury S, Frydenberg M, Horvath LJ, Joshua AM, Lawrence NJ, Marks JE, McCaffrey JE, McDermott R, McGannett M, North SA, Barnes F , Parulekar W, Pook DW, Reaume MN, Sandhu SK, Tan A, Tan TH, Thomson A, Vera-Badillo F, Williams SG, Winter D, Yip S, Zhang AY, Zielinski RR, Davis ID; Investigadores del ensayo ENZAMET y del Grupo de Ensayos de Cáncer Genitourinario y de Próstata de Australia y Nueva Zelanda. Supresión de testosterona más enzalutamida versus supresión de testosterona más terapia antiandrógena estándar para el cáncer de próstata metastásico sensible a hormonas (ENZAMET): un ensayo internacional, abierto y aleatorizado de fase III. Lanceta Oncol. 2023 abril;24(4):323-334. doi: 10.1016/S1470-2045(23)00063-3. PMID: 36990608.
- Harshman LC, Chen Y, Liu G, Carducci MA, Garrard D, Dresser R, Han N, García JA, Hussein M, Shiffrin D, Eisenberger M, Kohli M, Plimack ER, Cooney M, Vogelzang NJ, Pecos J, DePaola R , Sweeney CJ; ECOG-ACRIN 3805 Investigadores. El antígeno prostático específico de siete meses es un pronóstico del cáncer de próstata metastásico sensible a hormonas tratado con privación de andrógenos con o sin docetaxel. J Clin Oncol. 1 de febrero de 2018; 36 (4): 376-382. doi: 10.1200/JCO.2017.75.3921. Publicación electrónica del 20 de diciembre de 2017. PMID: 29261442; PMCID: PMC5805480.
- Hussain M, Tangen CM, Perry DL, Higano CS, Crawford ED, Liu G, Wilding G, Prescott S, Kanaga Sundaram S, Small EJ, Dawson NA, Donnelly PJ, Fenner PM, Vaishambayan UN Shellhammer BF, Quinn D, Raghavan D , Ely B, Moinpour CM, Vogelzang NJ, Thompson IM Jr. Privación androgénica intermitente versus continua en el cáncer de próstata. N Inglés J Med. 4 de abril de 2013; 368 (14): 1314-25. doi: 10.1056/NEJMoa1212299. PMID: 23550669; PMCID: PMC3682658.

«Solucionador de problemas. Gurú de los zombis. Entusiasta de Internet. Defensor de los viajes sin disculpas. Organizador. Lector. Aficionado al alcohol».